酶是用作特定反应的催化剂的蛋白质。通过提供具有较低活化能的替代反应,它们允许反应以更高的速率进行。值得注意的是,酶不会改变反应的均衡;他们只能提高速度。没有酶,因此反应仍然仍处于相同方向;然而,它会慢,往往会慢得多。酶通常会增加10之间的反应率5.10.7.时代。我们体内需要酶以进行特定的代谢反应。它们对它们的基板非常具体,就像一个钥匙特定于特定门。其基材的酶的特异性LED emilfischer在1894年提出所谓的“锁和关键”假设。“锁和关键”假设意味着酶是静态分子,它们不是静态分子。称为诱导合适的另一个机制是首选模型;根据该模型,酶在与底物结合时经历一致性变化,并且这些变化是催化必需的[1,2]。
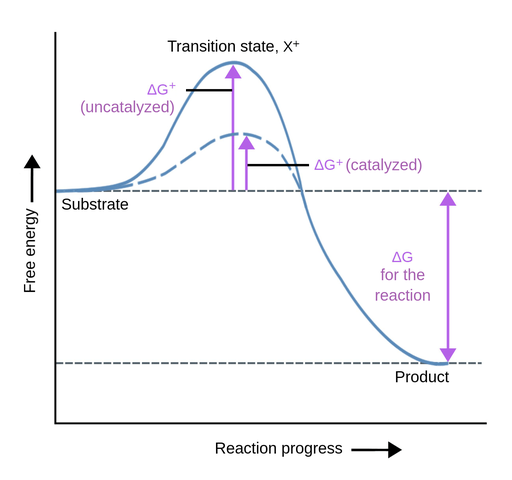
图1:从基材到产物的反应是从一个能量状态到另一个能量状态的转变。在基板和产品之间存在过渡状态。该状态具有比基板和产品的能量水平更高。催化剂将降低该能级,从而更容易达到过渡能量,这导致更快的反应。
酶如何降低激活能量?
酶可以增强其特定反应的速率存在许多不同的方式。当两个基质转化成一个或多个产物时,酶将结合两个基板,从而确保它们靠近附近并正确地朝向彼此定向。当反应发生而没有酶时,2个基板必须从正确的角度彼此碰撞,并且具有足够的能量(速度)以克服更高的激活能量。当基材被酶结合时,通过酶的结构克服这些挑战。酶(和一般催化剂)的重要特征是它们在反应过程中未使用。当酶催化反应时,它可以转换另一组底物。[1]
参考
Lehninger,Albert L。尼尔森,大卫湖;Cox,Michael M.(2008)。生物化学原理(第五次)。纽约,纽约:W.H.弗里曼和公司。ISBN 978-0-7167-7108-1。
阿特金斯,彼得w .;De Paula,Julio;弗里克曼,罗纳德(2009)。Quanta,物质和变化:物理化学的分子方法。牛津大学出版社。ISBN 978-0-19-920606-3。