Principios básicos de la reacción de eliminación E1
La eliminación E1 es un tipo dereacción de eliminaciónen química orgánica. Tiene lugar en dos pasos separados, pero la velocidad de la reacción está solo limitada por uno de los reactivos. La figura 1 ofrece un ejemplo de eliminación E1.
1)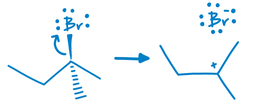
El grupo saliente (el bromuro), toma los electrones y se separa de la molécula principal, que se vuelve uncarbocatión. Los carbocationes no son estables, ¡por lo que ha de ocurrir alguna otra reacción subsecuente!
2)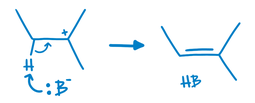
Una base abstrae un protón de la molécula principal, lo que la estabiliza a través de la formación de un enlace doble.
Figura 1:Ejemplo de los pasos 1 y 2 de la reacción de eliminación E1, utilizando 2-bromo-2-metilbutano como reactivo principal.
Factores importantes que influyen en la reactividad E1
Estos factores, por lo general, aumentan la reactividad de cara a una eliminación E1:
Un buengrupo salienteen la molécula principal.
Grado de sustitución: cuanto más sustituido está el carbocatión (potencial), más estable es y, por tanto, más susceptible de formarse es. De hecho, ¡E1 casi ocurre en exclusiva en átomos de carbono terciarios!
Base: una base fuerte que pueda abstraer el hidrógeno. Aunque, en realidad, E1 puede tener lugar hasta con una base débil.
Temperatura: la velocidad de las reacciones de eliminación suele aumentar con la temperatura. Cuando compiten con reacciones de sustitución, añadir calor a la reacción eliminará la ruta de eliminación.
El disolvente en el que tiene lugar la reacción puede tener un gran impacto. La manera en que afecta a las reacciones de eliminación excede el contenido de esta simulación, pero puedes consultaresta página如果您愿意版本联合国resumen de la manera en suelen clasificarse los disolventes.
Estereoquímica del producto de reacción
Como la reacción atraviesa un carbocatión planar intermediario, no hay selectividad específica del producto haciacisotrans, y el resultado suele ser una mezcla de ambos.