Un four fermé où la colonne peut être stockée dans un environnement à température contrôlée.

La température est un facteur important lors de la séparation de composés par CLHP. La colonne peut être placée dans un four fermé où la température peut être régulée.
La thermodynamique en CLHP
La rétention d'un soluté dans un système chromatographique est déterminée d'une part par l'ampleur du coefficient de distribution du soluté entre les deux phases, et d'autre part par la quantité de phase stationnaire disponible pour l'interaction du soluté. Le point important est que la constante d'équilibre est une quantité thermodynamique. Par conséquent, la relation suivante de la thermodynamique s'applique :
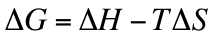
∆G représente l'énergie libre standard d'adsorption à la phase stationnaire, ∆H représente l'enthalpie standard d'adsorption à la phase stationnaire, ∆S représente l'entropie standard d'adsorption à la phase stationnaire et T représente la température du système.
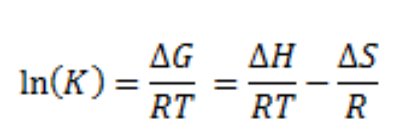
K represente la常数d 'equilibre pour la distribution entre la phase mobile et la phase stationnaire. R représente la constante des gaz et ln le logarithme naturel, tandis quek' représente le facteur de capacité. Comme le montre l'équation ci-dessus, l'énergie libre de Gibbs (∆G) peut être corrélée au facteur de capacité (k'). En développant l'équation de l'énergie libre de Gibbs, nous pouvons mesurer l'effet du changement de température sur le facteur de capacité.
Les avantages de fonctionner avec une température plus élevée
Il y a plusieurs avantages à faire fonctionner la séparation des composés à une température plus élevée. Outre la réduction des temps d'exécution, une augmentation de la température peut avoir d'autres effets bénéfiques. Lorsque la température augmente, la viscosité de la phase mobile diminue, ce qui entraîne des pressions plus faibles. Une viscosité plus faible de la phase mobile améliore également la diffusion dans le système chromatographique, ce qui donne des pics plus étroits. Simultanément, des temps de rétention plus courts génèrent des pics plus étroits. Des pics plus étroits signifient des pics plus élevés, en supposant la même masse d'échantillon sur la colonne, et donc des limites de détection plus basses. Si vous êtes satisfait de travailler à la pression d'origine, vous pouvez encore réduire le temps d'exécution en augmentant le débit avec des séparations isocratiques jusqu'à ce que la pression d'origine soit atteinte.
L'augmentation de la température accroît également la solubilité du composé. Lorsqu'un composé a une faible solubilité, il risque de précipiter et de boucher la colonne. Ce phénomène peut être évité en augmentant la température. Cependant, il faut également tenir compte du fait que la stabilité des composés dépend de la température, notamment pour les composés biologiques. Lorsque la température est trop élevée, ces composés peuvent se dégrader et vous ne serez pas en mesure d'obtenir une bonne séparation et une bonne mesure.
Ainsi, dans de nombreux cas, une augmentation de la température peut avoir de multiples avantages, à condition qu'il n'y ait pas de changements négatifs de la sélectivité.