Die Redoxreaktion Zwischen Zwei Chemischen SpeziesHängtvon von den jeweiligenstärkender reduktions- und氧化敏捷。Die Richtung der Reaktion Kann Anhand EinerReaktivitätsreihe,DieMoleküleNachIhrerStärkeals氧化 - Oder Reduktionsmittel ordnet,AbgeschätztOderanhand des des氧化还原Berechnet Werden。
在einerreaktivitätsreihewird das reaktiveremoleküldie die reduktionsreaktion durchlaufen,währenddas anderemoleküldie die oxiDationsReactionsReaktiondurchläuft。
füreinen Mathematischeren ansatz kann das das redoxential verwendet Werden。wenn das mit der formel berechnete zellpotity
eZelle=eKathode-e阳极
积极的伊斯特,贝德特死,dass die reaktion spontanabläuft和potentielle energie freigesetzt wird。Die Durch Diese Reaktionen Freigesetzte Energie Wird在Eine Andere Energieform Umgewandelt,Z。B.在Wärme中。EIN负面潜力Bedeutet,Dass Die ReaktionEnergieBenötigt,Um Abzulaufen,Und Dass sie nicht spontanabläuft。
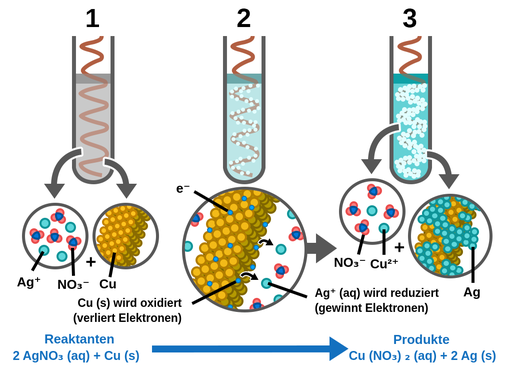
Abbildung 1:Redoxreaktion Zwischen Kupfer(Cu)Und Silber(AG)。kupfer ist dasstärkerereduktionsmittel und silber ist dasstärkere氧化米特尔在derreaktivitätsreiheund das势founty das势fürdie reaktion reaktion cu + 2 ag(否3)→Cu(否3)2+ 2ag iste= 0,8-0,34 = +0,46V。