米凯利斯常数K米的一个参数Michaelis-Menten方程.K米等于底物浓度对应的反应速率是½•V马克斯.K值低的酶米因此,实现其目的half-maximal速度底物浓度低,而K值高的酶米需要很高的底物浓度才能达到这个速度。实验表明,K米酶的浓度通常接近其底物的细胞浓度。对于包含2步的酶促反应,其中第二步是限速反应,K米近似等于ES络合物的解离常数。在这个例子中,是低K米意味着对底物的高亲和力;但是K的这种解释米只对几种酶有效[1]。
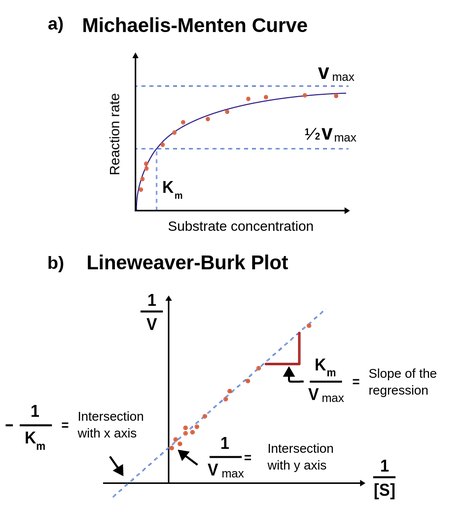
图1:图1.;Michaelis-Menten方程拟合了初始速率与底物浓度的关系。当底物浓度等于K时米时,反应速率为½*V马克斯.图1. b;拟合酶动力学数据集的双倒数变换的Lineweaver-Burk方程的插图。
Lineweaver-Burk方程
有几种确定Km的方法。最直接的方法是画出V0采用曲线拟合软件直接拟合Michaelis-Menten方程。然而,某些转换允许通过线性回归确定,这些转换在分析酶抑制时也很有用。有几种转换是可能的;然而,通过对Michaelis-Menten方程两边取倒数可以得到一个简单的解。这就得到了下面的表达式,称为Lineweaver-Burk方程:
1 / V0= 1 / V马克斯+ K米/ V马克斯•1 / [S]
这个方程显示,1/V的曲线0对1/[S]应给出一个可以用y轴截距为1/V的直线拟合的图马克斯和斜率K米/ V马克斯.因此,K米可以用线性回归得到。图1所示。b演示了如何解释Lineweaver-Burk图上的斜率和相交点。[1]
其他的转换
值得注意的是,Lineweaver-Burk转型并不是唯一的选择。例如,[S]/V0反对[S](哈内斯-伍尔夫的阴谋)也将导致一条直线[2]。然而,在本例中,我们将使用Lineweaver-Burk变换。
参考文献
Lehninger,阿尔伯特·l·;纳尔逊,大卫·l·;迈克尔·m·考克斯(2008)。生物化学原理(5日ed)。纽约,纽约州:W.H.弗里曼公司。ISBN 978-0-7167-7108-1。
Atkins, G.L.和Nimmo, I.A.(1975)拟合Michaelis-Menten方程的七种方法的比较。物化学。J。149, 775 - 777。