根据Michaelis-Menten方程,初始反应速率(V0)随着底物浓度的增加而增加[S]。底物浓度越低,反应速度越快,最终达到一个平台,接近最大速度V马克斯(图1)当酶达到饱和时,即存在足够多的底物,以确保几乎所有酶都是酶-底物复合物的一部分时,酶的初始速度达到最大。因为酶不可能完全饱和,V马克斯永远不会完全实现。V马克斯取决于两件事:什么转化率酶(k猫),酶的浓度[E][1]。
Vmax = [E]•kcat
因此,更高的[E]导致更高的V马克斯.营业额将在下面的页面中详细描述。
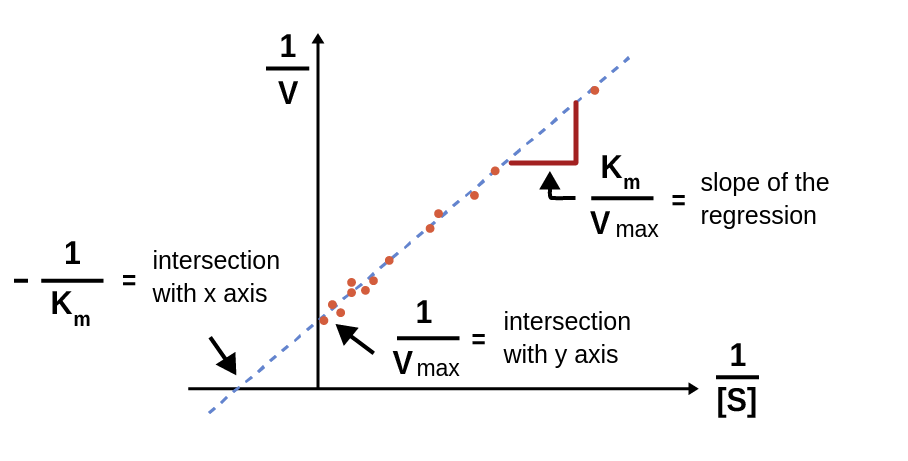
图1:拟合酶动力学数据集的双倒数变换的Lineweaver-Burk方程的插图。
确定V马克斯
就像k米, V马克斯可以用Lineweaver-Burk方程确定(图1):
1 / V0= 1 / V马克斯+ K米/ V马克斯•1 / [S]
根据这个方程,拟合到双倒数图上的直线的y轴截距为1/V马克斯V马克斯可以通过取这个截距[1]的倒数得到。
参考文献
- Lehninger,阿尔伯特·l·;纳尔逊,大卫·l·;迈克尔·m·考克斯(2008)。生物化学原理(5日ed)。纽约,纽约州:W.H.弗里曼公司。ISBN 978-0-7167-7108-1。