势能图显示了一个系统在发生化学反应时势能的变化。
的活化能(E一个)表示启动反应所需的最小能量。反应速率在很大程度上取决于活化能。活化能越低,反应速度越快。
的焓的变化反应物和生成物之间(在恒压下)的“热能”之差(ΔH)。
位于曲线顶端的分子或能垒叫做活化络合物或者是过渡态.
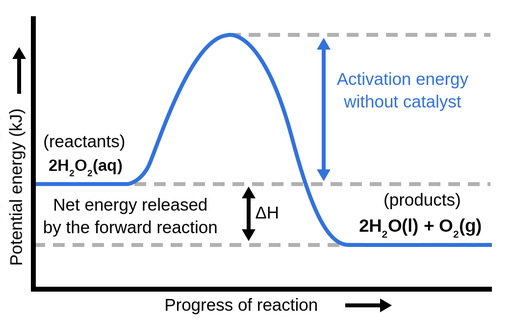
图1所示。反应2H时势能随反应进度的变化2O2- - - > 2 h2O + O2.这是一个放热反应.
势能图显示了一个系统在发生化学反应时势能的变化。
的活化能(E一个)表示启动反应所需的最小能量。反应速率在很大程度上取决于活化能。活化能越低,反应速度越快。
的焓的变化反应物和生成物之间(在恒压下)的“热能”之差(ΔH)。
位于曲线顶端的分子或能垒叫做活化络合物或者是过渡态.

图1所示。反应2H时势能随反应进度的变化2O2- - - > 2 h2O + O2.这是一个放热反应.