冰表
ICE代表“初始,变化,平衡”。这些表格对于计算平衡状态下的反应物和生成物的浓度很有用。
这三个步骤可以发生在溶解酸或碱在水中,例如。
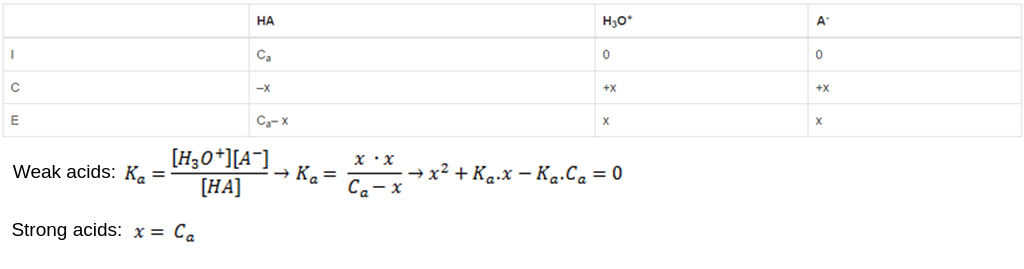
在这个表格中,C一个代表酸的初始浓度,x是反应的量(消失为负,形成为正)。这个金额可以从酸解离常数(K一个)用浓度代替平衡时得到的浓度(表e列),然后分离出x。
注意x可以近似于C一个当它是强酸时,因为它们是完全离解的。
ICE表也可用于一个反应的一个基地在水里。
ICE代表“初始,变化,平衡”。这些表格对于计算平衡状态下的反应物和生成物的浓度很有用。
这三个步骤可以发生在溶解酸或碱在水中,例如。
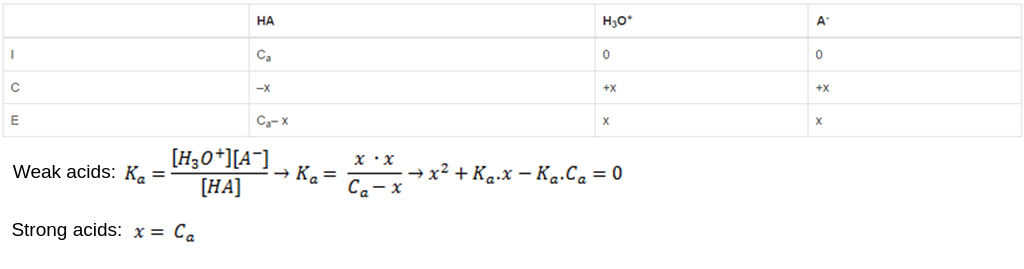
在这个表格中,C一个代表酸的初始浓度,x是反应的量(消失为负,形成为正)。这个金额可以从酸解离常数(K一个)用浓度代替平衡时得到的浓度(表e列),然后分离出x。
注意x可以近似于C一个当它是强酸时,因为它们是完全离解的。
ICE表也可用于一个反应的一个基地在水里。