化学結合(イオン結合および共有結合共有結合化合物)の形成には電子移動または電子共有のいずれかが関与します。化学結合の原子価殻電子価電子を可視化する1つの方法としてルイス構造を使用します。この
概念は1916年にギルバート・N・ルイスによって発表されました。
ルイス構造では、すべての原子価殻電子はそれぞれ1つの点として図示されます。孤立電子対は、元素記号の周りの2つの点として示されます。共有電子または孤立電子対を表すために直線を使用する場合が
あります。
ルイス構造の概念によれば、カリウム (K) と塩素 (K) の間のイオン結合の形成は、次のように定式化できます。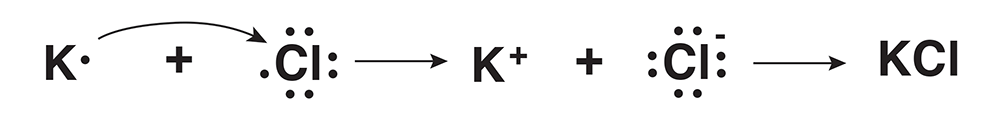
共有結合化合物のルイス構造の例はCl2です。
ルイス構造を作図する方法を学習しますLearn how to draw the Lewis structures。"