像在解释部分precedente苏尔chromatographie en phase liquide à haute performance, la séparation se déroule dans la colonne en raison des interactions entre l'analyte et les phases stationnaire et mobile.
Il existe un équilibre entre l'analyte et les deux phases. Plus l'analyte interagit avec la phase stationnaire, plus il restera dans la colonne. S'il interagit davantage avec la phase mobile, il restera moins longtemps dans la colonne. Le coefficient de partage (K) est utilisé pour mettre en relation la concentration de la substance à analyser dans chacune des deux phases, comme indiqué ci-dessous :
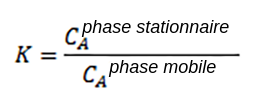
Kreprésente le coefficient de partage,CAphase stationnairereprésente la concentration molaire de l'analyte dans la phase stationnaire etCAphase mobilereprésente la concentration molaire de l'analyte dans la phase mobile. Plus l'analyte passe de temps dans la phase stationnaire, plus la valeurKest grande.
la force de dispersion de London
la force de dispersion de London est une faible interaction qui se produit entre des molécules non polaires.

Il existe différents types d'interactions entre les chaînes latérales des billes de la colonne et les analytes présents dans l'échantillon. L'une de ces interactions est la force de dispersion appelée "force de London". Il s'agit d'une faible interaction qui se produit entre deux molécules non polaires, c'est-à-dire deux molécules lipophiles. Cette force est présente entre deux dipôles instantanément induits, qui sont dus au mouvement des électrons dans les molécules. Si la phase stationnaire a des chaînes non polaires attachées au support inerte ( comme par exemple la chaîne C-18 vue dans la figure), les analytes avec des groupes non polaires (comme par exemple le stéarate de magnésium vu dans la figure) présenteront des forces de dispersion de London et resteront plus longtemps dans la colonne.